Veranstaltungen
Am Institut für Pharmazie und Lebensmittelchemie finden regelmäßig interessante Vorträge, Kolloquien und Fortbildungen zu aktuellen wissenschaftlichen Themen statt.
Wir sind nicht nur in der Forschung stark, sondern bilden auch Offizin-Apotheker fort und bieten unseren Doktoranden die Möglichkeit zur Weiterbildung zum Fachapotheker für Pharmazeutische Analytik und Pharmazeutische Technologie. Neben der Bayerischen Akademie für Klinische Pharmazie (Gründungsmitglieder sind die Professorinnen Petra Högger und Ulrike Holzgrabe), die sich um die Ausbildung von praktizierenden Apothekern in diesem Fach kümmert, gibt es die "Würzburger wissenschaftliche Winterfortbildung", einen jährlich stattfindenden Fortbildungsnachmittag, sowie regelmäßig Abendvorträge in Kooperation mit der Deutschen Pharmazeutischen Gesellschaft.
Die Vorträge sind für das Fortbildungszertifikat der Bayerischen Landesapothekerkammer mit 2 Punkten für Apotheker, PTA und Pharmazeuten im Praktikum anrechenbar.
DPhG-Vorträge
Beginn der Vorträge ist jeweils um 19.00 Uhr.
-
Der Vortrag am 28. April 2026 findet nur per ZOOM statt.
-
Die Vorträge am 19. Mai und 23. Juni 2026 finden „hybrid" statt:
-
in Präsenz im Seminarraum 01.005 im Institut für Pharmazie und Lebensmittelchemie am Hubland und
-
online per ZOOM.
-
Referenten und Vorträge im Sommersemester 2026
„Intelligenz im System: KI in der Medizin – und die unterschätzte Rolle der Apotheke"
„Vom Ende der Pharmazie, wie wir sie kennen“
„Arzneimitteltherapie – geht das auch ohne Fehler?“
Anmeldung
Um am ZOOM-Meeting teilnehmen zu können, wählen Sie den entsprechenden Link aus und folgen Sie den Anweisungen, um sich zu registrieren.
Danach erhalten Sie eine E-Mail zur Bestätigung inkl. des Meeting-Links.
So finden Sie den Veranstaltungsort:
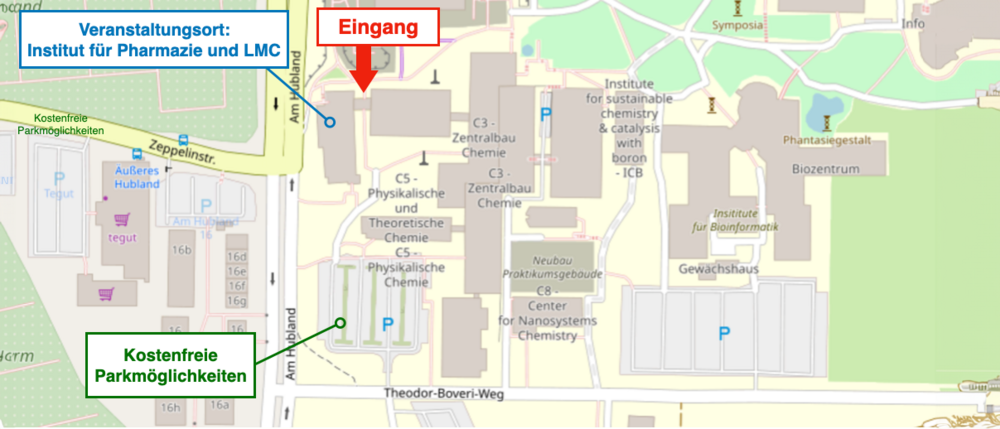
Das Institut für Pharmazie und LMC finden Sie direkt an der Straße "Am Hubland" an der Kreuzung zur Zeppelinstraße. Den Haupteingang erreichen Sie über den kleinen Weg links neben dem Gebäude in Richtung Mensa.
Der Seminarraum 01.005 befindet sich im 1. Stock, Lehrstuhl für Pharmazeutische Chemie, hinter der Glastür am Ende des kurzen Flures. Zusätzlich wird der Weg vom Haupteingang ausgehend beschildert sein.
27. Würzburger wissenschaftliche Winterfortbildung 2026
Termin: 7. Februar 2026, 15.00 Uhr
Programm
| 15.00 - 15.10 Uhr | Begrüßung und Einleitung in das Thema |
| Prof. Dr. Ulrike Holzgrabe (Institut für Pharmazie und LMC, Universität Würzburg) | |
| 15.10 - 16.00 Uhr | Wandel der Tumortherapie - von klassischen Chemotherapeutika zu zielgerichteter Tumortherapie |
| Prof. Dr. Y.-D. Ko (Comprehensive Cancer Center CIO Bonn, Johanniterkrankenhaus) | |
| 16.00 - 16.50 Uhr | AMTS bei oraler Antitumortherapie |
| Prof. Dr. Oliver Scherf-Clavel (Klinische Pharmazie, LMU München) | |
| 16.50 - 17.20 Uhr | Pause |
| 17.20 - 18.10 Uhr | Evidenzbasierte Komplementäre Verfahren in der Onkologie |
| Prof. Dr. Jutta Hübner (Innere Medizin, Universitätsklinikum Jena) | |
| 18.10 - 18.20 Uhr | Zusammenfassung |
Veranstaltungen der GDCh
Informationen zu Vorträgen im Rahmen der GDCh-Vortragsreihe finden Sie hier (externer Link zur Seite des Jungchemikerforums Würzburg).